熱運動
熱運動
この世のあらゆる物体は分子あるいは原子でできているわけですが、この分子、原子は常に揺れ動いています。乱雑に揺れ動いています。静止しているように見える場合でも微視的には揺れ動いています。この運動を熱運動といいます。熱運動はブラウン運動の原因となるものです。ブラウン運動というのは液体中に浮遊する微粒子がランダムに動き回る運動のことです 19世紀のイギリスの植物学者、ロバート・ブラウンが発見しました 。液体分子のランダムな衝突によって引き起こされます。
熱運動の激しさを熱といいます。熱というのは熱運動の運動エネルギーのことです。
極論をいいますと、熱というものに実体は無く、分子の運動の激しさを熱という言葉に言い換えただけです。 厳密には、分子の重心の運動以外に分子内の電子の位置エネルギーの変化なども考慮しなければなりません。また、熱という言葉はエネルギーが移動したときのみに使うべきだという考え方もあります。
温度
 熱運動の大きさを測る物差しの一つが、温度という尺度です。
熱運動の大きさを測る物差しの一つが、温度という尺度です。
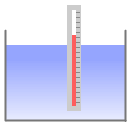
一般的な温度計は赤色に着色した灯油の膨張具合によって温度を測定します。
温度によって体積が膨張することを熱膨張といいます。分子の熱運動が原因です。
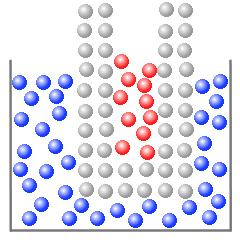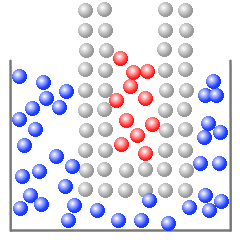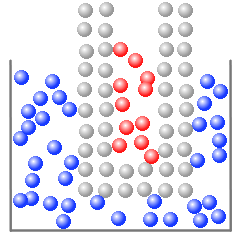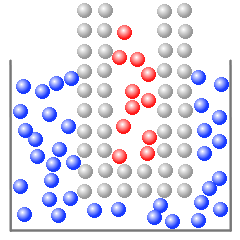 検査対象物の分子が熱運動をしていて、その分子が温度計のガラス管に当たり、ガラス分子の熱運動を激しくし、ガラス分子が赤色灯油の灯油分子の熱運動を激しくし、赤色灯油が膨張し、温度計の目盛りを指します。
検査対象物の分子が熱運動をしていて、その分子が温度計のガラス管に当たり、ガラス分子の熱運動を激しくし、ガラス分子が赤色灯油の灯油分子の熱運動を激しくし、赤色灯油が膨張し、温度計の目盛りを指します。
(左図のガラス分子は説明のため格子状に並んでいますが、実際のガラス分子の配列はもっと複雑です。)
温度の種類は、いくつかあります。
セルシウス温度
日本の日常生活でよく使われているのが、セルシウス温度です。セ氏温度(せしおんど)といったり、摂氏温度(せっしおんど)といったりもします 18世紀のスウェーデンの天文学者、アンデルス・セルシウスが考案しました。セルシウスさんが考案したので「セ氏」です。 。単位は [℃] あるいは [度] です。水が凍る温度と沸騰する温度が基準となっています。1気圧のもとでの純水の凝固点が 0℃、沸点が 100℃ です。
絶対温度
熱運動が全て停止する温度を基準とするのが、絶対温度です。ケルビン温度ともいいます 19世紀のイギリスの物理学者ケルビン卿にちなんで名付けられました 。単位は [K] ケルビン です。セルシウス温度でいうところの -273.15℃ になると、熱運動というものは完全に停止します。そして、これ以下の温度はありません。この世で一番低い温度が -273.15℃ です。この温度を絶対零度といいます。この温度を 0K とし、目盛りの間隔をセルシウス温度と同じにした温度が絶対温度です。
絶対温度を \(T\) [K]、セルシウス温度を \(t\) [℃] とすると、\(T\) = \(t\) + 273.15 です。
-273.15 ℃ = 0 K
0 ℃ = 273.15 K
100 ℃ = 373.15 K
その他の温度単位
英語圏の国で古い慣習として使われているのが、ファーレンハイト温度です。華氏温度(かしおんど)ともいいます 18世紀のドイツの物理学者ガブリエル・ファーレンハイトが提唱しました。ファーレンハイトの中国音訳が「華倫海特」で、華さんが提唱したので「華氏」です。 。単位は [℉] です。人間の体温が基準になっています。物理では使われません。
物質の三態
物質には3種類の状態、固体、液体、気体があり、物質の三態といいます。温度や圧力によって物質の状態は変化します。
固体
 分子は規則正しく並んでいて、互いに強い分子間力で結びついています。ですので固体の物体は形を一定に保つことができます。各分子は所定位置で乱雑な振動をしています。
分子は規則正しく並んでいて、互いに強い分子間力で結びついています。ですので固体の物体は形を一定に保つことができます。各分子は所定位置で乱雑な振動をしています。
液体
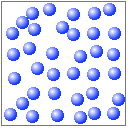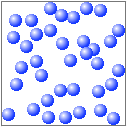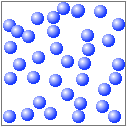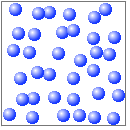 固体に比べて、分子の熱運動が激しく、分子間力は弱くなっています。分子間の距離はあまり変わりませんが、各分子の位置は自由に変わります。そのため、体積は大きく変わることはありませんが、形は自由に変わります。容器の形に応じて形を変えることができます。
固体に比べて、分子の熱運動が激しく、分子間力は弱くなっています。分子間の距離はあまり変わりませんが、各分子の位置は自由に変わります。そのため、体積は大きく変わることはありませんが、形は自由に変わります。容器の形に応じて形を変えることができます。
気体
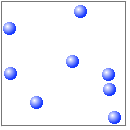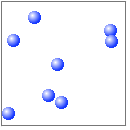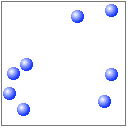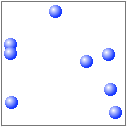 液体に比べてさらに分子の熱運動が激しくなります。分子間力はほとんどはたらかず、分子間の距離は大きくなり、各分子は自由に運動し、体積は温度や圧力によって大きく変化します。気体はその体積に比べて分子の占める割合がとても小さいので、気体の種類が異なっても共通の性質が見られ、法則化することができます。
液体に比べてさらに分子の熱運動が激しくなります。分子間力はほとんどはたらかず、分子間の距離は大きくなり、各分子は自由に運動し、体積は温度や圧力によって大きく変化します。気体はその体積に比べて分子の占める割合がとても小さいので、気体の種類が異なっても共通の性質が見られ、法則化することができます。
状態変化
以下で説明することは化学の教科書に詳しく載ってます。
固体 ⇄ 液体
固体が熱をもらって液体に変化することを融解といいます。この変化が起こるときの温度を融点(融解点)といいます。融解に必要な単位質量当たりの熱を融解熱といいます。
液体が熱を放出して固体に変化することを凝固(固化)といいます。この変化が起こるときの温度を凝固点といいます。凝固するときに放出する単位質量当たりの熱を凝固熱といいます。
(厳密さを求めなければ)融点=凝固点であり、融解熱=凝固熱です(絶対値が同じで正負の符号が逆)。
水の融点(氷点)は 0℃ です。氷と水を混ぜたものは温度が 0℃ です。0℃ の温度を作るのは簡単ということです。
液体 ⇄ 気体
液体が熱をもらって気体に変化することを蒸発(気化)といいます。この変化が起こるときの温度を沸点といいます。蒸発に必要な単位質量当たりの熱を蒸発熱(気化熱)といいます。
気体が熱を放出して液体に変化することを凝縮(液化)といいます 日常生活でいうところの結露とは、凝縮のことです 。この変化が起こるときの温度の名前は特にありません。凝縮するときに放出する単位質量当たりの熱を凝縮熱といいます。
蒸発熱=凝縮熱です。
水の沸点は 100℃ です。沸騰中の水の温度は 100℃ です。つまり水と水蒸気を混ぜたものは温度が 100℃ です。100℃ の温度を作るのは簡単です。
固体や液体の表面だけで起こる気化を蒸発といい、液体の内部からも起こる気化を沸騰といいます。
固体 ⇄ 気体
固体が熱をもらって気体に変化することを昇華(気化)といいます。この変化が起こるときの温度を昇華点といいます。昇華に必要な単位質量当たりの熱を昇華熱といいます。
気体が熱を放出して固体に変化することを凝華といいます
新しく作られた言葉です。
昔は固体から気体への変化も気体から個体への変化もどちらも昇華と呼称していました。
。この変化が起こるときの温度の名前は特にありません。この変化のときに放出する熱の名前も特にありません。
ドライアイス(冷やして固体にした二酸化炭素)を常温常圧に置くと、昇華して気体の二酸化炭素になります。 液体の二酸化炭素というものはあまり見かけませんが、二酸化炭素を気体から液体にするには強い圧力を掛ける必要があります。
潜熱
融解熱や蒸発熱のことを潜熱といいます。正負を考えなければ凝固熱や凝縮熱や昇華熱も全部潜熱です。物質に潜んでいるとみなせる熱です。
固体から液体、液体から気体に変化するときは潜熱を吸熱します。外部からエネルギーを取り入れます。
冷却器の多くにこの原理が応用されています
液体から固体、気体から液体に変化するときは潜熱を発熱します。外部にエネルギーを放出します。
クーラーの室外機の原理です