内部エネルギー
内部エネルギーとは
ある1つの物体に着目したときに、その物体の運動エネルギーと位置エネルギーとの和を力学的エネルギーといいます。
物体というものは分子(あるいは原子)で構成されていて、その分子は動いている(運動エネルギーがある)し、分子と分子の間には力がはたらいている(位置エネルギーがある 分子間に力がはたらくとすると、その距離の大小によって位置エネルギーがあるとみなせます。『重力による位置エネルギー』、『弾性力による位置エネルギー』、『静電気力による位置エネルギー』参照。 )ので、個々の分子には力学的エネルギーがある、といえます。しかし、何万、何億という個数の分子をひとまとめにしてみたときには、それらの分子の力学的エネルギーのことを内部エネルギーと呼びます。
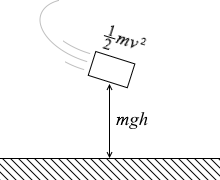 :物体の力学的エネルギー = \({\large\frac{1}{2}}mv^2 + mgh\)
:物体の力学的エネルギー = \({\large\frac{1}{2}}mv^2 + mgh\)
 :物体の内部エネルギー = 物体を構成する分子のエネルギー
:物体の内部エネルギー = 物体を構成する分子のエネルギー
この内部エネルギーは上の力学的エネルギーとは関連性はありません。内部エネルギーを考えるときは、物体内部のエネルギーのことだけを考えます。物体の速さや物体の高さのことは考えません。 領域内のことだけを考えて領域外のことを考えないとき、この領域のことを「系」といいます。大学物理の用語です。『慣性系⋅非慣性系』参照。
単原子分子の理想気体の内部エネルギー
理想気体では、分子間力は無いものとみなすので、分子間力による位置エネルギーは無いと考えます。よって、分子の運動エネルギー(=熱)の総和がそのまま理想気体の内部エネルギーとなります。
単原子分子の理想気体の分子1個の運動エネルギーは
\({\large\frac{1}{2}}m\overline{{v}^2} = {\large\frac{3}{2}}kT = {\large\frac{3}{2}}⋅{\large\frac{R\ }{N_{\rm A}}}⋅T\)
であり、この分子の個数が 1mol あるとすると、つまり \(N_{\rm A}\)倍すると、
\({\large\frac{1}{2}}m\overline{{v}^2}⋅N_{\rm A}\) = \({\large\frac{3}{2}}⋅{\large\frac{R\ }{1}}⋅T\)
であり、分子の個数が \(n\) [mol] あるとすると、さらに \(n\)倍して、
\(n⋅{\large\frac{1}{2}}m\overline{{v}^2}⋅N_{\rm A} = n⋅{\large\frac{3}{2}}⋅{\large\frac{R\ }{1}}⋅T\)
であり、これを \(U\) [J] とおくと< \(U\) の語源は分かりません 、以下のようになります。
単原子分子の理想気体の内部エネルギー
\(\boldsymbol{U = {\large\frac{3}{2}}nRT}\)
単原子分子の理想気体の内部エネルギーは、物質量(≒分子の個数)と絶対温度のみに比例します。物質の種類は無関係です。
物質量が一定(≒分子の個数が一定≒質量が一定)ならば、絶対温度が \(ΔT\) [K] 変化したときの内部エネルギーの変化量 \(ΔU\) [J] は以下のようになります。
\(ΔU = {\large\frac{3}{2}}nRΔT\) \(ΔU = {\large\frac{3}{2}}nR(T + ΔT) - {\large\frac{3}{2}}nRT = {\large\frac{3}{2}}nRΔT\)